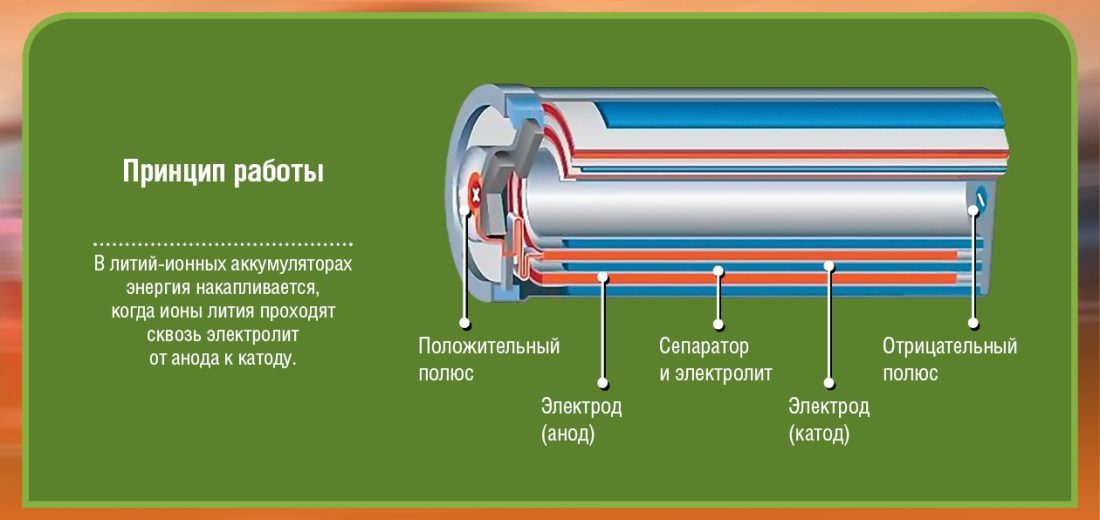
Цахилгаан тээврийн хэрэгслийн лити ион батерей хэрхэн ажилладаг вэ?
Өөр нэг нийтлэлээс бүх машинууд тоноглогдсон хар тугалга батерейны ажлыг харсны дараа одоо цахилгаан тээврийн хэрэгсэл, ялангуяа түүний лити батерейны ажиллах зарчмыг харцгаая ...

Ханхүү
Ямар ч төрлийн батерейны нэгэн адил зарчим нь ижил хэвээр байна: тухайлбал, химийн эсвэл бүр цахилгаан урвалын үр дүнд эрчим хүч (энд цахилгаан) бий болгох, учир нь хими нь үргэлж цахилгааны хажууд байдаг. Үнэн хэрэгтээ атомууд өөрсдөө цахилгаанаас бүрддэг: эдгээр нь цөмийн эргэн тойронд эргэлддэг электронууд бөгөөд ямар нэгэн байдлаар атомын "бүрхүүл" эсвэл бүр "арьс" -ыг бүрдүүлдэг. Чөлөөт электронууд нь нэг атомаас нөгөө атом руу шилжихэд цаг хугацаа зарцуулдаг (түүнтэй холбоогүй) нисдэг арьсны хэсгүүд гэдгийг мэддэг учраас энэ нь зөвхөн дамжуулагч материалын хувьд (электронуудын давхаргын тоо, электронуудын тооноос хамаарна) сүүлчийн сум тутамд).
Дараа нь бид химийн урвалаар атомуудаас "арьсны хэсэг" (тиймээс түүний цахилгааны зарим хэсгийг) авдаг бөгөөд цахилгаан үүсгэдэг.

суурь
Юуны өмнө бидний нэрлэдэг хоёр туйл (электрод) байдаг катод (+ терминал: лити-кобальт исэлд) ба анод (терминал -: нүүрстөрөгч). Эдгээр туйл бүр электроныг хазайдаг (-) эсвэл (+) татдаг материалаар хийгдсэн байдаг. Бүх зүйл усанд автсан электролит цахилгаан үүслийн үр дүнд химийн урвал (материалыг анодоос катод руу шилжүүлэх) боломжтой болгоно. Богино холболтоос зайлсхийхийн тулд эдгээр хоёр электрод (анод ба катод) хооронд хаалт суурилуулсан.
Батерей нь хэд хэдэн эсээс бүрдэх бөгөөд тус бүр нь диаграммд харагдаж байгаа зүйлээс бүрддэг гэдгийг анхаарна уу. Жишээлбэл, би 2 вольтын 2 эсийг хуримтлуулах юм бол батерейны гаралт дээр зөвхөн 4 вольт байх болно. Хэдэн зуун кг жинтэй машиныг хөдөлгөөнд оруулахын тулд хэдэн эс хэрэгтэйг төсөөлөөд үз дээ ...
Хогийн цэг дээр юу болж байна вэ?
Баруун талд литийн атомууд байдаг. Тэдгээрийг нарийвчлан харуулсан бөгөөд шар зүрх нь протоныг, ногоон зүрх нь тэдний тойрог замд байгаа электронуудыг төлөөлдөг.
Батерейг бүрэн цэнэглэх үед бүх литийн атомууд анод (-) талд байрлана. Эдгээр атомууд нь цөмөөс (хэд хэдэн протоноос бүрддэг) 3-ын эерэг цахилгаан хүч, электронууд нь 3-ийн сөрөг цахилгаан хүч (нийт 1, учир нь 3 X 3 = 1) байдаг. ... Тиймээс атом нь 3 эерэг, 3 сөрөг (электроныг татахгүй, хазайдаггүй) тогтвортой байдаг.
Бид литийн электроныг салгаж авдаг бөгөөд энэ нь зөвхөн хоёроор нь болж хувирдаг: дараа нь энэ нь +-д татагдаж, хуваалтаар дамждаг.
Би + ба - терминалуудын хооронд холбоо барих үед (тиймээс би батерей ашиглах үед) электронууд зайны гаднах цахилгааны утасны дагуу - терминалаас + терминал руу шилжих болно. Гэсэн хэдий ч эдгээр электронууд нь литийн атомуудын "үс" -ээс гардаг! Үндсэндээ эргэн тойронд эргэлдэж буй 3 электроноос 1 нь тасарч, атомд 2-хон электрон үлддэг.Гэнэт түүний цахилгаан хүч тэнцвэржихээ больсон бөгөөд энэ нь мөн химийн урвал үүсгэдэг. Мөн литийн атом болж байгааг анхаарна уу лити ион + учир нь одоо эерэг байна (3 - 2 = 1 / Цөм нь 3, электрон нь 2, учир нь бид нэгийг алдсан. Нэмэхэд өмнөх шиг 1 биш 0 болно. Тиймээс энэ нь төвийг сахисан байхаа больсон).
Тэнцвэргүй байдлаас үүссэн химийн урвал (электроныг эвдэж гүйдэл үүсгэсний дараа) нь илгээхэд хүргэнэ. лити ион + бүх зүйлийг тусгаарлах зориулалттай ханаар дамжуулан катод руу (терминал +). Төгсгөлд нь электрон ба ионууд + талдаа төгсдөг.
Урвалын төгсгөлд зай цэнэггүй болно. Одоо + ба - терминалуудын хооронд тэнцвэр бий болсон бөгөөд энэ нь одоо цахилгаанаас сэргийлдэг. Үндсэндээ цахилгаан гүйдэл үүсгэхийн тулд химийн / цахилгааны түвшинд сэтгэлийн хямралыг өдөөх зарчим юм. Үүнийг бид гол гэж ойлгож болно, энэ нь налуу байх тусам урсах усны эрч хүч чухал байх болно. Нөгөөтэйгүүр, гол нь тэгшхэн байвал урсахаа болино, энэ нь батерейны цэнэггүй болсон гэсэн үг юм.
Цэнэглэх үү?
Цэнэглэх нь электронуудыг чиглэл рүү нь шахах замаар үйл явцыг эргүүлж, сорох замаар илүү ихийг зайлуулахаас бүрдэнэ (энэ нь голын урсгалыг дахин ашиглахын тулд голын усыг дүүргэхтэй адил юм). Тиймээс батерейны бүх зүйл цэнэггүй болохоос өмнөх шигээ сэргээгддэг.
Үндсэндээ бид цэнэгээ алдахдаа химийн урвалыг ашигладаг бөгөөд цэнэглэхдээ анхны зүйлээ буцааж өгдөг (гэхдээ үүний тулд танд эрчим хүч, тиймээс цэнэглэх станц хэрэгтэй).
Өмсөх үү?
Лити батерейнууд нь манай автомашинд олон зууны турш ашиглагдаж ирсэн хуучин сайн хар тугалганы хүчлийн батерейг бодвол хурдан элэгддэг. Электролит нь электродууд (анод ба катод) шиг задрах хандлагатай байдаг ч электродууд дээр хуримтлал үүсдэг бөгөөд энэ нь ионуудын нэг талаас нөгөө тал руу шилжихийг бууруулдаг ... Тусгай төхөөрөмж нь танд үүнийг зөвшөөрдөг. ашигласан батерейг тусгай аргаар цэнэглэх замаар сэргээх.
Боломжит мөчлөгийн тоог (цэнэглэх + бүрэн цэнэглэх) ойролцоогоор 1000-1500 гэж тооцдог тул хагас циклээр цэнэглэх үед 50-ээс 100% биш харин 0-100% байна. ХАЛААЛТ нь литийн ион батерейг маш ихээр гэмтээдэг бөгөөд хэт их хүч хэрэглэх үед халах хандлагатай байдаг.
Мөн үзнэ үү: Цахилгаан машиныхаа зайг хэрхэн хэмнэх вэ?
Хөдөлгүүрийн хүч ба зай ...
Дулаан дүрслэгчээс ялгаатай нь түлшний савны хүч чадалд нөлөөлдөггүй. Хэрэв та 400 морины хүчтэй хөдөлгүүртэй бол 10 литрийн багтаамжтай савтай байх нь маш богино хугацаанд ч гэсэн 400 морины хүчтэй болоход саад болохгүй ... Цахилгаан машины хувьд энэ нь огт адил биш юм! Хэрэв зай хангалттай хүч чадалгүй бол хөдөлгүүр бүрэн хүчин чадлаараа ажиллах боломжгүй болно ... Энэ нь зарим загварт хөдөлгүүрийг хэзээ ч хязгаарлах боломжгүй (эзэмшигч нь хуурч, том калибрын батарей нэмэхгүй бол) тохиолддог. !).
Одоо цахилгаан мотор хэрхэн ажилладагийг олж мэдье
Бүх сэтгэгдэл, хариу үйлдэл
Дерниер сэтгэгдэл оруулсан:
Мао (Огноо: 2021, 03:03:15)
маш сайн ажил
Ил Ж. 1 энэ сэтгэгдэлд үзүүлэх хариу үйлдэл:
- Админ САЙТЫН УДИРДЛАГА (2021-03-03 17:03:50): Энэ сэтгэгдэл бүр ч сайхан байна 😉
(Таны бичлэгийг баталгаажуулсны дараа коммент хэсэгт харагдах болно)
Сэтгэгдэл бичих
Үйлдвэрлэгчдийн зарласан хэрэглээний тоо хэмжээний талаар та ямар бодолтой байна вэ?
